(griech.) Unmittelbarer und vollständiger Übergang vom schmelzflüssigen in den festen Zustand. Mit anderen Worten: Liquidus- und Soliduslinie fallen zusammen. Diese Erstarrung führt zu einem feinkörnigen und gleichmäßigen Gefüge, das aus zwei Kristallarten besteht. Eine eutektische Legierung hat immer den niedrigsten Schmelzpunkt und die besten Gießeigenschaften.

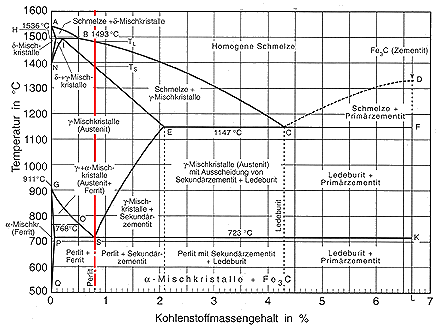
Das Eisen-Kohlenstoff-Diagramm
zeigt bei einer Temperatur von 1.145°C und einem Massengehalt von 4,3 % C ein
E. Das Gefüge, das sich aus der Schmelze bildet, heißt Ledeburit (nach seinem
Entdecker A. Ledebur). Das Eisen-Kohlenstoff-Diagramm zeigt eine ähnliche
Erscheinung auch bereits bei 0,83 % C und einer Temperatur von 723 °C. Hier
scheiden sich die beiden Phasen Ferrit und Zementit aus dem Austenit aus und
bilden ein Gefüge namens Perlit. Dieses "kleine Eutektikum" wird
Eutektoid genannt. Entsprechend spricht man auch vom eutektoidischen,
untereutektoidischen (< 0,83 % C) oder übereutektoidischen (> 0,83 % C)
Stahl.